- 디지털기기 사용 증가로 근시 확산… 임상 설계·평가 기준 구체화로 산업 경쟁력 강화
- 국제 기준 맞춘 신속 개발 지원… “의료기기 안전성과 효과성 확보에 기여 기대”
식품의약품안전처(처장 오유경)가 근시 교정용 콘택트렌즈의 국내 개발과 신속한 제품화를 지원하기 위해 ‘각막 굴절 교정용 콘택트렌즈 임상시험계획서 작성 가이드라인’을 제정·발간했다. 이번 지침은 관련 제품의 임상 설계, 평가 기준, 자료 작성 방법 등을 표준화해 산업계와 연구기관이 임상시험을 보다 효율적으로 진행하도록 돕는 것이 목표다.
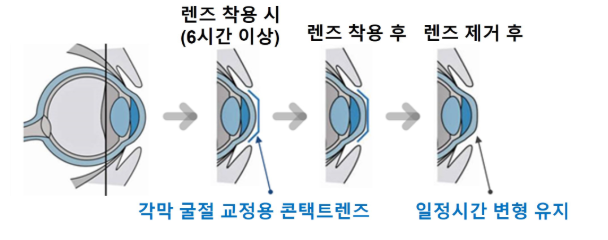
각막 굴절 교정용 콘택트렌즈는 야간 수면 시 착용하면 렌즈가 각막 중심부를 눌러 형태를 일시적으로 바꾸는 방식으로, 낮 동안 근시를 교정하는 하드렌즈다. 일명 ‘드림렌즈(Ortho-K Lens)’로 불리며, 소아·청소년층을 중심으로 시력 교정 수요가 빠르게 증가하고 있다. 디지털 기기 사용 급증과 온라인 학습 확산으로 청소년 근시 유병률이 상승하면서, 관련 시장도 빠르게 확대되는 추세다.
식약처는 이번 가이드라인을 통해 ▲임상시험계획서 주요 항목 및 작성 방법 ▲국제 기준에 부합하는 임상 설계 예시 ▲시험 중 평가 기준과 효과성 판정 지표 등을 구체적으로 제시했다. 그동안 국내 기업들은 제품개발 단계마다 임상 설계나 평가 기준에 불확실성이 커 임상 진행 지연과 해외 인증의 어려움을 겪는 경우가 많았다. 이에 따라 이번 제정은 국내 산업계의 개발 효율성과 글로벌 진출 기반을 동시에 강화할 수 있을 것으로 기대된다.
식약처는 이번 가이드라인이 국민생활과 밀접한 의료기기 개발을 촉진하고, 혁신 기술이 적용된 제품이 빠르게 시장에 진입할 수 있도록 지원하는 중요한 전환점이 될 것으로 전망했다. 또한 기술 발전 속도에 맞춰 규제 과학 기반의 안전성·효과성 검증 체계를 강화해, 국민 건강 보호와 함께 국내 의료기기 산업의 국제 경쟁력 확보에 기여하겠다고 밝혔다.









